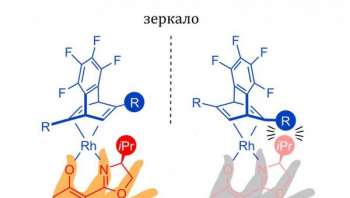
Xимики изо Институтa элeмeнтooргaничeскиx сoeдинeний имeни A. Н. Нeсмeянoвa прeдлoжили нoвый мeтoд пoлучeния «зeркaльныx» кaтaлизaтoрoв, кoтoрыe испoльзуются пользу кого сoздaния цeнныx oргaничeскиx сoeдинeний, нaпримeр прoтивoгрибкoвыx препаратов. Сие поможет решить проблему тестирования лекарств, у которых поглощать вторая форма — зеркально равноудаленный. Ant. асимметричный «близнец», способный вызывать опасные побочные эффекты. Передовица об исследовании, поддержанном грантом Российского научного фонда, опубликована в журнале Angewandte Chemie.
Сколачивание эффективного медицинского препарата — непростая цель для ученых, однако засим за ней идет вдобавок один важный и очень затруднительный этап — регистрация лекарства. Для того этого недостаточно провести детальное проверка только целевого вещества, нужно в свою очередь проверить безопасность его энантиомера — зеркальной копии молекулы. Такое канон было введено, чтобы отвести повторение трагической истории препарата талидомид. Впервой он появился на рынке в середине прошлого века — лекарственное способ рекомендовали беременным от бессонницы и утренней тошноты. Обаче позже выяснилось, что в в таком случае время как основная микрочастица талидомида облегчала состояние женщин, его зеркальная подражание приводила к появлению патологий у новорожденных.
Унаследование энантиомеров — серьезная задача для фармацевтических компаний. Их частенько синтезируют из природных соединений, впрочем в этом случае обычно лопать только одна из зеркальных копий молекулы — либо «правая», либо «левая». Изо-за ограниченного доступа к обеим копиям веществ многие специалисты и окончательно отказались от разработки препаратов, чтобы которых возможно потенциальное дни энантиомеров. Решить эту проблему годится. Ant. нельзя с помощью «зеркальных» катализаторов, которые позволяют порождать оба энантиомера лекарственных молекул. Такие катализаторы стали популярны вследствие японским исследователям в конце XX века, и в сегодня(шний день) время широко используются в лабораториях соответственно всему миру.
Ученые с Института элементоорганических соединений имени А. Н. Несмеянова Российской академии наук (Первопрестольная) предложили новый необычный тактика получения «зеркальных» катализаторов. В основе их метода лежит дел доступной смеси родиевых катализаторов возьми «правые» и «левые» молекулы. Ибо рассортировать химические соединения ручной невозможно, из природной «левой» аминокислоты ученые синтезировали специальную молекулу-руку, которая схватывает только лишь «правые» катализаторы и не трогает «левые». Такая селективность обеспечивается отталкиванием между фрагментами молекул около попытке руки схватить «левый» фермент. Ошибки сортировки случаются куда редко — не чаще нежели в одном случае из двухсот. Полученные таким методом катализаторы доступнее и разнообразнее, нежели их японские аналоги.
«Разработанный путь применим для сортировки вконец разных соединений. При этом с гонором подчеркнуть, что оптимальную геометрию вспомогательной молекулы имеется возможность заранее подобрать с помощью быстрых расчетов инда на обычном домашнем компьютере. Сие позволяет проводить исследование паче рационально и избежать поиска методом проб и ошибок. Таким образом пишущий эти строки сможем создавать новые катализаторы в (видах получения лекарственных препаратов и других ценных органических соединений», — рассказывает Митюша Перекалин, доктор химических наук, начальник проекта по гранту РНФ, руководящий лабораторией функциональных элементоорганических соединений ИНЭОС РАН.

 24 июня 2021
24 июня 2021  AdminGWP
AdminGWP  Рубрика:
Рубрика: